————————————————————————

『ゲノム編集を考える』(中編)
1.種無しトマトにするために、トマト細胞に挿入されたプラスミドの構造
〇ゲノム編集する際に挿入されるプラスミド(細胞分裂によって娘細胞へと引き継がれるDNA分子※)の構造は特に公表されていないのですが、河田氏はそのプラスミド遺伝子の構造を調べてみて驚きました。発光クラゲの遺伝子とか抗生物質耐性遺伝子が当たり前のように使われているではないですか。これらは選別する際に必要な遺伝子として挿入されていたのです。
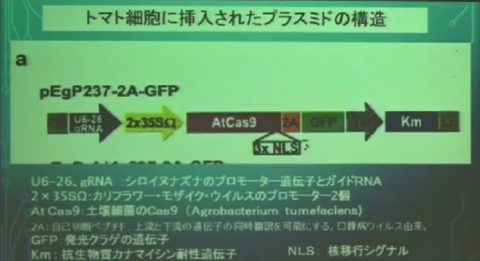
〇トマト細胞に挿入されたプラスミドの構造
・U6-26,gRNA...プロモーター(転写開始の部分)、ガイドRNA(ターゲット遺伝子への誘導)
・2x35SΩ...プロモーター2個(大豆やコーンの遺伝子組み換えでもよくスイッチとして使われる)
・AtCas9...土壌細菌のCas9(これがターゲット遺伝子を破壊する)
・2A...口蹄疫ウィルスの遺伝子
・GFP...発光クラゲの遺伝子
・Km...抗生物質カナマイシン耐性遺伝子
※プラスミドというDNA分子は、いわばトロイの木馬のようなものと考えるとわかりやすいかもしれません。(しんしん丸説。当たらずといえども遠からず!かと?)
トロイの木馬の中には、ターゲットとなる遺伝子の元へと誘導するガイドRNAがいたり、そのターゲット遺伝子を破壊するCas9という工作員がいたり、照明係のクラゲ発光遺伝子や敵の攻撃から身を守るための抗生物質耐性遺伝子がいるのです。破壊工作員である彼らはトロイの木馬とともにトマト国へと運び込まれるのであった。
トロイの木馬の中には、ターゲットとなる遺伝子の元へと誘導するガイドRNAがいたり、そのターゲット遺伝子を破壊するCas9という工作員がいたり、照明係のクラゲ発光遺伝子や敵の攻撃から身を守るための抗生物質耐性遺伝子がいるのです。破壊工作員である彼らはトロイの木馬とともにトマト国へと運び込まれるのであった。
※遺伝子組み換えでも抗生物質耐性遺伝子は使われています。抗生物質であるグリホサートへの耐性を持たせるためです。そしてグリホサートに漬けこんで生き残るものが遺伝子組み換えに成功したものとして選別するのです。こういう遺伝子を持つ作物は、育てているときに除草剤ラウンドアップ(主成分はグリホサート)をたっぷりかけても枯れません。(モンサント方式は種・農薬・肥料の3点セット売り)そしてこうした作物を食べることで、残留したグリホサートが人体の中の腸内細菌の働きを阻害して、様々な肉体疾患、精神疾患を引き起こすということがわかっています。
2.アグロバクテリウム法(遺伝子の導入方法)
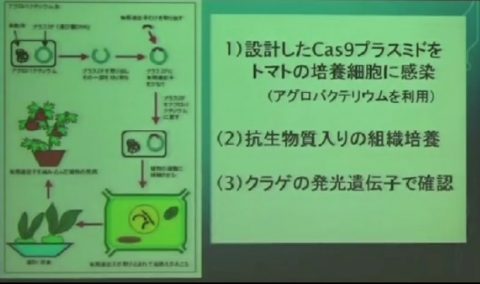
・制限分解酵素(DNAを切断する)Cas9の入ったプラスミドの遺伝子をトマトの培養組織に感染させます。
↓
・抗生物質入りの組織を培養します。
↓
・クラゲの発光遺伝子で確認します。
※これは、ゲノム編集にてすぺての遺伝子をノックアウトできるわけではないからです。ですから、ノックアウトできたものを選別する必要があるのです。そのために抗生物質への耐性機能と発光機能を組み込むわけです。
3.発光する組織を集める
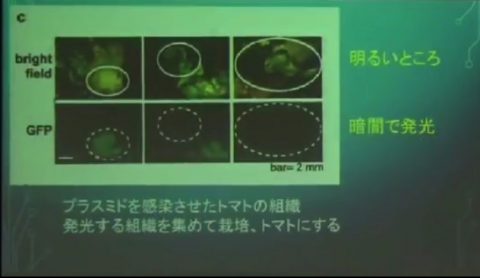
・こうして発光する組織を集めます。すなわち、ゲノム編集でノックアウトできた組織だけを選別して栽培するというわけです。
4.未授精種子なしトマトに含まれることになる遺伝子

・カリフラワー・モザイク・ウイルスのプロモーター遺伝子
・抗生物質カナマイシン耐性遺伝子
・発光クラゲの遺伝子
・Cas9遺伝子
※これらは本来異質な遺伝子です。
中国では、受精卵にゲノム編集することで先天異常の病気を治す実験がおこなわれました。赤ちゃんを育てたらそのうち暗闇で光るようになる?かもしれないのです。大丈夫なのでしょうか?
中国では、受精卵にゲノム編集することで先天異常の病気を治す実験がおこなわれました。赤ちゃんを育てたらそのうち暗闇で光るようになる?かもしれないのです。大丈夫なのでしょうか?
5.ゲノム編集した肥大豚にもこのような遺伝子が!

・ペニシリン耐性遺伝子
・ストレプトマイシン耐性遺伝子
・発光クラゲ遺伝子
・鉄粉を結合した遺伝子
※さらにてっとり早いという理由から、鉄粉の遺伝子をプラスミドに組み込む方法も今では多く使われているようです。磁場で分別できるというわけです。
6.RNA編集技術

・遺伝子を変えないでmRNAを編集することで、タンパク質だけを変換するというRNA編集技術が、昨年2017年の末に発表されました。
・2018年の4月には、RNAの検知紙も開発されました。つい最近のことです。
・実用化はまだとはいえ、それだけ浸透してきています。
※遺伝子を変えてしまうゲノム編集への批判に対して、遺伝子を変えるわけではないというRNA編集の登場ではありますが。
7.ゲノム編集とRNA編集の違い

・ゲノム編集はDNAを変えてしまうため、永久に効果が継続する(遺伝子治療などにおける根本的治療)ということになりますが、その点RNA編集は一過的といえます。用途はまだ未開発です。
〇後編につづく。
ちょっと一息!
河田氏はtRNAの働き、DNAの塩基配列がアミノ酸配列に翻訳される仕組みを専門に研究されていたそうです。tRNAと関連する酵素を高純度に精製することに成功した時、実は米の研究者が半年早く成し遂げていて、その米の研究者はノーベル賞を受賞したのでした!と、河田氏はにこやかに話されました。
今回のこうした警告は、もっと大切な、"地球"への貢献ともいえるのではないでしょうか!!危険な子供の火遊びを止めさせるためにも。
 画像の出典::pixabay[cc0]
画像の出典::pixabay[cc0]




ゲノム編集は、遺伝子組み換え技術よりも「早く」「効率よく」生物を改変できる新しいテクノロジーとしてとしての側面ばかりが取り上げられていますが、河田氏は、公表されていないそのプラスミド(後述)を見て驚いたわけです。なんと抗生物質耐性遺伝子が使われているではないですか!ゲノム編集に成功した組織を容易に選別できるように、ゲノム編集時に本来の目的とする遺伝子とは関係のない、抗生物質耐性遺伝子や発光クラゲの遺伝子を組み込んでいるのです。このことにより選別時に、グリホサートに漬けて、遺伝子組み換えに成功した組織だけが生き残り、その中から光る組織だけを容易に選別することができるというわけです。そして、すべてのゲノム編集にはこの選別の目的のために抗生物質耐性遺伝子や光る遺伝子などが組み込まれているというのです。これはゲノム編集が危険な理由の一つです。
さらにゲノム編集は、目的以外の遺伝子(オフターゲット遺伝子)を破壊するという危険性もあります。ですからターゲット以外の遺伝子の発現をモニターする必要があるわけですが、それは安全審査の対象外とされています。(従来の遺伝子組み換えでもこのことは対象外です)
つまりゲノム編集は、ターゲット遺伝子を特定できるといわれていますが(これですらオフターゲット問題がある)、技術的には従来の遺伝子組み換えと大差ないということです。このように、ゲノム編集には遺伝子組み換えと同様の危険性の問題がつきまとっているわけです。
要するに、実用化などもってのほか!ということです。
こうした中、米国農務省(USDA)はゲノム編集による遺伝子操作には従来のGMOに対してのような規制はいらないとしました。こうした判断をするということは、この問題を必要悪として容認しているということになるのではないでしょうか。(※)
こうした危険を野放しにしている現状に、河田氏は警鐘を鳴らしているわけです。
(※)USDAは、それまでは反対が多いために許可してこなかった遺伝子組み換え小麦に対して、ゲノム編集による遺伝子組み換えの栽培を許可しました。これにより今後、ゲノム編集の作物が一気に市場に出回ることが危惧されます。そしてこれに呼応するかのように、日本では小麦におけるグリホサートの規制値が大幅に緩和されました。(5ppmから30ppmへ。大豆は20ppmで据え置き)ですから今後は小麦(パン、麺類、様々な加工食品)によるグリホサートの影響が大いに懸念されるわけです。